Gianluca Trifirò1, 2, Salvatore Crisafulli2, 3, Gabriele Puglisi3, Giorgio Racagni2, 4, Luca Pani2, 5, 6, 7
1Dipartimento di Diagnostica e Sanità Pubblica, Università di Verona
2Società Italiana di Farmacologia (SIF)
3Dipartimento di Scienze Biomediche, Odontoiatriche e delle Immagini Morfologiche
e Funzionali, Università di Messina
4Dipartimento di Scienze Farmacologiche e Biomolecolari, Università di Milano
5Dipartimento di Scienze Biomediche, Metaboliche e Neuroscienze
Università di Modena e Reggio Emilia
6Dipartimento di Psichiatria e Scienze Comportamentali, Leonard M. Miller School
of Medicine – Università di Miami
7VeraSci, Durham, USA
Tendenze nuove, Numero Speciale n.01 2021; 147-158: DOI: 10.32032/TENDENZENS20210111.PDF
 Scarica Pdf
Scarica Pdf
1. La digitalizzazione in sanità
La rivoluzione digitale sta determinando, da almeno dieci anni, trasformazioni radicali in tutti i settori della società e ultimamente inizia ad avere i suoi impatti soprattutto in ambito sanitario. Due fattori fondamentali sono responsabili di questa vera e propria rivoluzione: i) la quantità di dati di salute generati da ogni singolo paziente; ii) la capacità computazionale sia in termini di archiviazione che di analisi. Tutto ciò non solo sta modificando i tempi e gli spazi degli stessi concetti di salute e malattia, ma sta anche trasformando il comportamento dei pazienti e i processi diagnostici e terapeutici(1). Secondo l’Osservatorio Innovazione Digitale in Sanità, in Italia nel 2018 la spesa digitale in campo sanitario è cresciuta del 7%, per un totale di 1.4 miliardi di euro annui(2).
Con il termine “Salute Digitale” (o digital health o eHealth) si intende l’uso di diverse tecnologie digitali al fine di supportare ed erogare servizi sanitari a sostegno della salute e del benessere degli individui, non necessariamente ancora malati. All’interno di questa vasta definizione rientrano molteplici tecnologie, tra le quali telemedicina, social media, applicazioni (App), dispositivi indossabili, smartphone e terapie digitali. Tali tecnologie rappresentano nuove opportunità per affrontare le sfide che, a livello globale, si presentano sempre più frequentemente, con l’obiettivo di migliorare la qualità dei servizi sanitari e mettendo al centro il singolo paziente (3). Questo settore non è ancora provvisto di un vocabolario standard, ma sono tre le macro-definizioni che categorizzano le tecnologie utilizzate in ambito sanitario: Salute Digitale, Medicina Digitale e Terapie Digitali (Digital Therapeutics o DTx). Nella definizione generale di Salute Digitale rientrano quelle tecnologie, come le App o Web App, che supportano gli utenti nel modificare i propri stili di vita e perseguire obiettivi di benessere, generando dati sanitari che possono supportare le attività di ricerca e la pratica clinica. Con il termine “Medicina Digitale”, invece, si intende una categoria di tecnologie digitali, sviluppate sulla base di evidenze cliniche, atte a realizzare interventi a favore della salute umana. Infine, la definizione di terapie digitali comprende tutte quelle tecnologie digitali che offrono interventi terapeutici evidence-based con lo scopo di prevenire, gestire o curare un problema medico o una malattia(3).
2. Il ruolo della digitalizzazione nella terapia farmacologica
La maggior parte delle applicazioni tecnologiche utilizzate dai pazienti è rappresentata dai cosiddetti programmi di supporto (Patient Support Programmes – PSPs) digitali. Si tratta di interventi di natura organizzativa o altro, privi di attività terapeutica, ma finalizzati ad affiancare i pazienti per gestire meglio il decorso della loro malattia, comprendere bene le condizioni di salute e/o fornire consulenza sull’andamento della malattia.I PSPs digitali sono principalmente rappresentati da App personalizzate, intente a promuovere l’aderenza alle terapie farmacologiche, favorire le comunicazioni tra pazienti e professionisti sanitari, offrire strumenti per il monitoraggio della malattia e, più in generale, promuovere il coinvolgimento del paziente nella cura quotidiana della propria salute. Considerando la loro capacità di raccogliere dati clinici tramite diari clinici e/o questionari, i PSPs possono essere utili anche per la ricerca, nel rispetto della privacy dei pazienti. In quanto applicazioni prive di attività terapeutica, molto raramente vengono sottoposte a sperimentazioni cliniche(3).
Diversamente dai PSPs, le Medicine Digitali sono prodotti farmaceutici in cui il farmaco da assumere è integrato con un sensore che viene attivato dopo l’ingestione e il cui fine ultimo è quello di garantire l’aderenza del paziente alla terapia. Le nanotecnologie farmaceutiche hanno smesso di essere parole da mistero iniziatico e sono entrate nel mercato dei prodotti “ingeribili”. Questi piccolissimi sensori trasmittenti possono essere formulati all’interno di una capsula o durante la preparazione industriale di una compressa e, una volta arrivati nello stomaco, grazie al pH acido, si attivano e trasmettono informazioni circa il loro percorso digestivo e quindi sulle funzioni del tratto gastroenterico e sull’assorbimento del principio attivo con cui sono stati associati. Il tutto si manterrebbe soltanto a livello di curiosità tecnologica se non fosse che la Food and Drug Administration (FDA) ha concesso la registrazione al primo prodotto combinato con questo tipo di sensori alla fine del 2017(4). Il nome commerciale è Abilify MyCite, sviluppato dall’azienda farmaceutica giapponese Otsuka che produce l’antipsicotico Aripiprazolo (®Abilify appunto), in collaborazione con Proteus Digital Health. Con il consenso del paziente il sensore, una volta ingerito, comunica con un “cerotto” ricevente e l’informazione è quindi trasmessa ad uno smartphone o a un tablet dello stesso paziente o di un’altra persona. Lo scopo finale è quello di misurare l’aderenza terapeutica in individui adulti affetti da psicosi primarie come la schizofrenia o episodi maniacali o misti nelle diagnosi di sindromi affettive bipolari di tipo I (figura 1). Tuttavia questa tecnologia non ha ricevuto molti consensi, determinando una grave crisi economica dell’azienda sviluppatrice; le motivazioni del fallimento possono probabilmente essere ricercate nella tipologia di pazienti ai quali questa tecnologia è rivolta, notoriamente poco aderenti alla terapia, e in alcune criticità di natura etica quale la supposta deumanizzazione dei pazienti, ridotti allo stato di “persone farmaceutiche”(5), oppure dal fatto che il ricevitore esterno rappresentava un limite tecnologico che, nel mondo di bluetooth, non era ammissibile. Il 17 luglio 2020 Otsuka ha infatti ritirato la domanda di autorizzazione presentata all’Agenzia Europea dei Medicinali (EMA)(6).
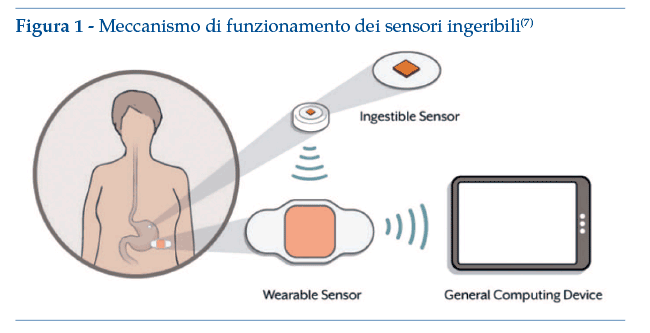
Un altro esempio di Medicina Digitale è rappresentato dalla tecnologia Propeller, sviluppata per i pazienti affetti da asma o broncopneumopatia cronica ostruttiva. In questo caso, il sensore viene applicato direttamente sull’inalatore e registra automaticamente dove, quando e con quale frequenza viene utilizzato il farmaco. Queste informazioni vengono successivamente inviate ad una App sullo smartphone(8). Approvato per l’utilizzo il 7 luglio 2020, Propeller è il primo sensore ad essere autorizzato in Europa.
Sebbene le terapie digitali dal punto di vista regolatorio siano classificate tra i Dispositivi Medici, le loro caratteristiche di ricerca, sviluppo e delivery sono assimilabili a quelle del farmaco. A differenza dei PSPs e delle “medicine digitali”, le terapie digitali sono infatti sviluppate attraverso una sperimentazione clinica controllata, sottoposte ad un percorso di approvazione per specifiche indicazioni d’uso da parte delle agenzie regolatorie, possono essere rimborsate e prescritte dal medico. Ciò che differenzia una terapia digitale da un farmaco convenzionale è il principio attivo, che non è più rappresentato da un’entità chimica o biologica, ma da algoritmi e software. Come i farmaci convenzionali, anche le terapie digitali presentano degli eccipienti, quali ad esempio moduli per gratificare il paziente, promemoria per l’assunzione della terapia digitale e delle terapie complementari, e moduli per mettere in contatto il paziente con il proprio medico e con altri pazienti con la medesima indicazione. All’interno del panorama delle tecnologie digitali sanitarie, le terapie digitali costituiscono una categoria indipendente di prodotti evidence-based la cui funzione primaria è quella di erogare interventi terapeutici generati da software, per prevenire, gestire o trattare un disturbo o una malattia(9). Le terapie digitali possono incorporare funzionalità aggiuntive che permettono l’integrazione con piattaforme sanitarie, la possibilità di fornire interventi per valutare l’aderenza terapeutica e di accoppiarsi con devices, sensori o dispositivi indossabili. Inoltre, permettono di generare terapie personalizzate, ottimizzando l’intervento in funzione delle caratteristiche individuali del paziente, attualizzando anche a livello digitale la cosiddetta “medicina personalizzata”(10).
Le terapie digitali possono generare interventi terapeutici sia in autonomia che in associazione a farmaci convenzionali, integrando l’innovazione tecnologica basata sull’utilizzo di software e algoritmi con la terapia farmacologica. Le terapie digitali definite stand-alone operano in maniera autonoma in quanto progettate come interventi atti a modificare i comportamenti disfunzionali di un paziente, sostituendosi alla terapia farmacologica. Un esempio di questo uso in “autonomia” è riscontrabile nell’ambito della psicoterapia dell’insonnia, della depressione, come anche del disturbo da deficit di attenzione e iperattività (ADHD) e della schizofrenia, dove lo sviluppo di diversi software che simulano modelli terapeutici cognitivo-comportamentali o psicoeducativi ha migliorato l’esito clinico dei pazienti, con un coinvolgimento diretto degli stessi nella gestione della patologia(10). L’associazione delle terapie digitali con i farmaci convenzionali, definibile come augment o add-on, può invece essere utile per migliorare l’efficacia clinica, la sicurezza e l’aderenza terapeutica degli interventi farmacologici associati, attraverso un lavoro congiunto fra dispositivi e farmaci. Per combinazione o combo intendiamo invece la condizione nella quale farmaco e terapia digitale vengono studiate come una “combinazione precostituita” attraverso uno sviluppo clinico che ha l’obiettivo di dimostrare la superiorità della combinazione rispetto al solo farmaco(11).
Le terapie digitali rappresentano una nuova opportunità principalmente per il trattamento di patologie croniche associate a stili di vita e comportamenti disfunzionali in cui la terapia convenzionale risulta soltanto parzialmente efficace. Le terapie digitali hanno il potenziale di correggere tali comportamenti disfunzionali, stimolando il coinvolgimento e la partecipazione attiva del paziente e fornendo informazioni e supporto nella gestione della patologia. Per questo motivo, esse risultano particolarmente adatte all’erogazione di terapie che normalmente si svolgono tramite incontri faccia a faccia, quali terapie cognitivo-comportamentali (CBT) e ipnoterapia clinica. Le indicazioni terapeutiche delle terapie digitali ad oggi approvate sono infatti rappresentate da malattie mentali, malattie metaboliche e dipendenze. L’erogazione di tali interventi terapeutici tramite dispositivi digitali può presentare diversi vantaggi, ad esempio: (i) un accesso facilitato alla terapia, anche durante il tempo libero e non soltanto limitatamente all’incontro con lo psicoterapeuta; (ii) la personalizzazione della terapia sulla base degli esiti e dei progressi osservati; (iii) una qualità consistente della terapia digitale, rispetto alla qualità estremamente variabile della terapia faccia a faccia con lo psicoterapeuta.
3. Agenzie regolatorie e terapie digitali
La prima terapia digitale ad ottenere l’approvazione dalla FDA nel 2017 è stata reSET®, una App sviluppata dall’azienda Pear Therapeutics, seguita nel 2018 da reSET-O®. reSET e reSET-O sono due esempi di terapie digitali da prescrizione (PDT) indicate, rispettivamente, per il trattamento del disturbo da uso di sostanze da abuso e della dipendenza da oppioidi. Si tratta di interventi erogati tramite App per dispositivi mobili che utilizzano la CBT nota come community reinforcement approach (CRA), originariamente sviluppata per la dipendenza da alcol e cocaina.
Nel giugno del 2020 la FDA ha approvato la commercializzazione di EndeavourRx, il primo game-based digital therapeutic device di Akili Therapeutics, per migliorare l’attenzione dei bambini con disturbo da deficit di attenzione e iperattività (ADHD). EndeavourRx è indicata per pazienti di età compresa tra 8 e 12 anni con ADHD ed è destinata all’uso come parte di un programma terapeutico che può includere terapie cliniche, farmaci e programmi educativi(12). EndeavourRx è basata su Akili Selective Stimulus Management (SSMETM), una tecnologia progettata per l’attivazione mirata di specifici circuiti neuronali, quindi per il trattamento di malattie con disfunzioni cognitive associate.
SomrystTM è una terapia digitale approvata nel 2020 dalla FDA per il trattamento dell’insonnia a carattere cronico, che utilizza l’intervento cognitivo-comportamentale (CBT-I); CBT-I è stato raccomandato dalle linee guida dell’American Academy of Sleep Medicine come trattamento di prima linea per persone che soffrono di insonnia cronica(13). SomrystTM fornisce inoltre informazioni sulla progressione dell’insonnia attraverso il monitoraggio del trattamento da parte del medico e degli operatori sanitari per mezzo di una dashboard che raccoglie dati metrici relativi al sonno, specifiche cliniche come l’Insomnia Severity Index (ISI) e valutazioni sulla qualità di vita dei pazienti con il Patient Health Questionnaire 8 (PHQ-8).
OleenaTM è la prima terapia digitale sviluppata in ambito oncologico ed approvata nel 2019 dalla FDA(14). È un’applicazione mobile PDT, progettata per aiutare i pazienti oncologici nella gestione dei sintomi e consentirne il monitoraggio in remoto da parte dei team sanitari. OleenaTM fornisce raccomandazioni personalizzate per la gestione della sintomatologia grazie ad algoritmi evidence-based. Questa terapia richiede una cooperazione tra operatore sanitario e paziente, in quanto la configurazione del dispositivo, in funzione delle specifiche cliniche del paziente, avviene inizialmente ad opera dell’operatore sanitario, e successivamente il paziente registrerà direttamente in OleenaTM i sintomi avvertiti e associati alla patologia oncologica.
Nel Regno Unito, il National Institute for health and Care Excellence (NICE), prima della Brexit, aveva creato un gruppo di lavoro guidato dal Servizio Sanitario inglese, il cui obiettivo era quello di rendere più semplice alle aziende e ai commissari la comprensione di quali fossero le evidenze utili per la valutazione degli strumenti digitali, rispondendo contemporaneamente sia alle esigenze del Servizio Sanitario che a quelle dei pazienti, ed accelerando i processi regolatori(15). Ora questa iniziativa deve essere considerata extra-territoriale rispetto all’Europa. Finora sono tre le terapie digitali raccomandate per l’utilizzo dal NICE, ma ancora non approvate: Deprexis, un dispositivo medico interattivo su base online che affianca il trattamento dei pazienti con depressione unipolare o disturbi depressivi dell’umore(16); Space from Depression, anche questo un programma online per il trattamento della depressione da utilizzare, sotto la supervisione di un terapista, come alternativa alla CBT convenzionale(17); BDD-NET, un programma online per il trattamento dei disturbi moderati-severi da dismorfismo corporeo(18).
Ad oggi, nessuna terapia digitale da prescrizione è autorizzata in Italia o nella maggior parte dei Paesi europei. Nel vecchio Continente, il sistema regolatorio relativo alle tecnologie digitali è ancora immaturo e mancano normative specifiche volte a valutare questi strumenti, garantire la sicurezza dei dispositivi e l’integrità dei dati raccolti. Da un punto di vista regolatorio, in Europa e negli Stati Uniti le terapie digitali vengono classificate all’interno dei dispositivi medici(19-21).
Per poter essere autorizzate all’immissione in commercio, è fondamentale che tali terapie vengano inquadrate da un punto di vista regolatorio, e che quindi siano opportunamente distinte dalle applicazioni per salute e benessere. Poiché, a differenza di queste ultime, le terapie digitali devono essere in grado di determinare un effetto terapeutico, per essere definite tali, è necessario che vengano fornite evidenze di efficacia e sicurezza prima che possano essere autorizzate all’immissione in commercio. Risulta quindi necessario definire, da un punto di vista regolatorio, la tipologia di terapia digitale per poter stabilire quali e quanti studi clinici siano necessari per poter approvare la sua commercializzazione.
5. Criticità
Nonostante i documentati aspetti positivi, le terapie digitali non sono esenti da criticità. Si tratta generalmente di tecnologie recenti e ancora in piena fase di sviluppo, per le quali non è sempre semplice condurre sperimentazioni cliniche in grado di generare sufficienti evidenze di sicurezza ed efficacia clinica. Gli endpoint digitali che vengono utilizzati nei trial clinici per le terapie digitali sono differenti da quelli dei trial clinici tradizionali, e la loro validazione risulta difficoltosa a causa dell’assenza di un gold standard. Inoltre, le caratteristiche tecniche della terapia digitale potrebbero essere aggiornate rapidamente durante il corso del trial, e la tecnologia stessa potrebbe diventare obsoleta ancor prima che la sperimentazione sia completata. È necessario, quindi, che queste terapie vengano sottoposte a diversi studi clinici rigorosi in tempi rapidi, per generare solide evidenze scientifiche in maniera tempestiva(22).
La mancanza di una normativa specifica volta a garantire la sicurezza di questi dispositivi e la qualità dei dati raccolti rappresenta un ulteriore ostacolo per lo sviluppo delle terapie digitali. La sorveglianza post-marketing dell’efficacia e della sicurezza delle Digital Therapeutics, in particolare nei confronti di possibili effetti avversi quali la dipendenza dalle terapie stesse, o la loro pseudo-specificità, rappresenta quindi un’attività fondamentale destinata ad avere un ruolo sempre maggiore con la progressiva introduzione delle terapie digitali nella pratica clinica(3). Più in generale, la dimensione della sicurezza di queste tecnologie è un argomento di particolare importanza. Nello studio clinico STARS-ADHD, il 6.7% dei soggetti trattati con AKL-T01 (Endeavour) ha manifestato eventi avversi, rispetto a 1.8% dei pazienti in trattamento con controllo attivo(23). Complessivamente gli eventi avversi documentati negli studi condotti con Endeavor hanno riguardato il 9.3% dei pazienti, comprendendo stati di frustrazione, mal di testa, reazioni emotive, vertigini, nausea ed aggressività(24).
Inoltre, la digitalizzazione della salute e del sistema sanitario determina una maggiore educazione e responsabilizzazione del paziente, promuovendone l’autogestione e il coinvolgimento nei processi decisionali di cura; questo processo, tuttavia, deve essere personalizzato e avvenire in maniera strutturata. Un eccessivo empowerment del paziente potrebbe impattare negativamente sul rapporto con il medico: sebbene infatti queste tecnologie possano permettere un dialogo costante tra clinico e paziente, esiste il rischio che un eccessivo ricorso alla tecnologia possa tendenzialmente ridurre la necessità di un rapporto diretto con lo specialista e ancor di più con il medico di famiglia.
Un’altra importante criticità associata all’utilizzo di queste tecnologie, e specificamente dei dispositivi indossabili (wearable devices), è rappresentata dalla gestione e condivisione dei dati dei pazienti. Sebbene la digitalizzazione dell’assistenza sanitaria stia procedendo lentamente, la quantità di dati utilizzabili a livello di paziente è aumentata notevolmente nell’ultimo decennio, e risulta pertanto necessario garantire la privacy e la security dei dati dei pazienti per supportare una corretta diffusione delle terapie digitali(25). Negli Stati Uniti, la gestione dei dati ottenuti tramite dispositivi medici è regolamentata dall’Health Insurance Portability and Accountability Act, che prevede la necessità di ottenere il consenso del paziente per la raccolta e la condivisione dei dati. Tuttavia, i dati ottenuti da questi dispositivi possono essere condivisi in modo criptato ed aggregato, senza un esplicito accordo su chi avrà accesso ai dati. Nell’Unione Europea, le nuove disposizioni del Regolamento generale sulla protezione dei dati (GDPR) non fanno distinzioni tra i vari dispositivi digitali, ma riguardano tutti i dati generati dai dispositivi indossabili o App di salute e benessere. Inoltre, l’Unione Europea richiede finalità chiaramente definite per l’utilizzo dei dati, il consenso del paziente per il riutilizzo e la condivisione dei dati, e consente ai pazienti di revocare il proprio consenso in qualsiasi momento.
6. Prospettive future
Alla luce della crescente digitalizzazione del mondo sanitario, con un valore sul mercato, per le sole terapie digitali, che si stima essere pari a circa 9.64 miliardi di dollari nel 2026(26), cominciano a prospettarsi interessi crescenti riguardo l’aspetto regolatorio e i processi di ricerca e sviluppo di queste tecnologie. La crescita economica del settore delle terapie digitali potrà raggiungere o superare quella del farmaco convenzionale, consentendo inoltre un maggiore accesso a patient-reported real-world data. Nel corso degli ultimi anni, molte imprese farmaceutiche hanno iniziato a cooperare con imprese tecnologiche per lo sviluppo di terapie digitali. Da queste collaborazioni derivano importanti opportunità di sviluppo ed innovazione. L’incremento della mole di dati relativi ad ogni aspetto della terapia e del paziente/utilizzatore, e l’elaborazione di sistemi statistico-predittivi sempre più raffinati, in uno scenario futuro, potranno consentire una maggiore personalizzazione del trattamento medico e la valutazione dell’effectiveness e della sicurezza di queste terapie ed eventuali farmaci associati. Inoltre, l’utilizzo di queste terapie in combinazione con farmaci convenzionali, con medesima indicazione e diverso meccanismo d’azione, può determinare effetti additivi o sinergici in termini di efficacia e tollerabilità, e rappresentare l’opzione a maggior valore terapeutico.
Il coinvolgimento del paziente nei processi decisionali di cura e nella gestione della propria salute dovrà tuttavia essere tale da preservare il rapporto diretto con il medico curante, il cui ruolo, se saprà cogliere appieno le potenzialità di queste terapie aggiuntive, resterà fondamentale per una corretta valutazione e gestione clinica della terapia, seppur conformandosi ad una maggiore indipendenza del paziente. Sarà pertanto compito del prescrittore educare il paziente ad utilizzare correttamente queste terapie, per evitare il ricorso ad autodiagnosi e cure fai-da-te, e l’aumento del carico emotivo dei pazienti più fragili.
What is known
• La Salute Digitale offre nuove opportunità per affrontare le criticità del sistema sanitario e migliorare la qualità dell’offerta, ponendo al centro il singolo paziente e mirando alla personalizzazione della cura
• C’è un’attenzione crescente della comunità clinica e scientifica nonché delle agenzie regolatorie alla digitalizzazione in sanità ed ancor più specificamente allo sviluppo di terapie digitali propriamente dette e di strumenti digitali a supporto di terapie farmacologiche convenzionali, come testimoniato dall’approvazione e commercializzazione di alcune di queste tecnologie
• Seppur le terapie digitali dal punto di vista regolatorio siano classificate tra i dispositivi medici, le loro caratteristiche di ricerca, sviluppo e delivery sono assimilabili a quelle del farmaco. In quanto tali, esse devono essere sviluppate attraverso una sperimentazione clinica controllata e sottoposte ad un percorso di approvazione per specifiche indicazioni d’uso da parte delle agenzie regolatorie, per poter essere eventualmente rimborsate e prescritte dal medico
• Le terapie digitali rappresentano una nuova opportunità terapeutica principalmente per il trattamento di alcune patologie croniche associate a stili di vita e comportamenti disfunzionali in cui la terapia farmacologica risulta soltanto parzialmente efficace.
What is uncertain
• Dal punto di vista regolatorio, le terapie digitali sono inquadrate come dispositivi medici; tuttavia, in Europa non esiste ancora un iter regolatorio chiaro e dedicato che tenga conto delle specificità di queste terapie che richiedono tempi di sviluppo più rapidi rispetto ai farmaci convenzionali
• La considerevole quantità di dati sensibili generata da queste tecnologie pone diversi quesiti relativamente all’utilizzo di tali dati e alla tutela della privacy dei pazienti
• Non è ancora definito come possa avvenire e quale istituzione debba prendersi carico del monitoraggio post-marketing della sicurezza delle terapie digitali.
What we recommend
• Qualunque terapia digitale va integrata in un programma di cura che deve essere deciso dal medico curante e condiviso con il paziente
• Come per i farmaci tradizionali, dopo l’introduzione in commercio di ogni terapia digitale è essenziale rivalutarne attentamente il profilo beneficio-rischio in real world setting
• È fondamentale armonizzare a livello globale le procedure di sviluppo ed approvazione alla commercializzazione delle terapie digitali.
Riferimenti bibliografici
1. Pani L. Radical singularities and future of Pharmacology. Pharmadvances 2019; http://www.pharmadvances.com/radical-singularities-and-the-future-of-pharmacology.
2. Innovazione digitale in sanità: i risultati 2019 [Internet]. Available from: https://www.impresasanita.it/it/articles/20190531/innovazione_digitale_in_sanita_i_risultati_2019.
3. Recchia G, Capuano MD, Mistri N, Verna R. Digital Therapeutics-What they are, what they will be. Acta Sci Med Sci 2020; 4: 1-9.
4. Food and Drug Administration. FDA approves pill with sensor that digitally tracks if patients have ingested their medication [Internet]. 2017. Available from: https://www.fda.gov/news-events/press-announcements/fda-approves-pill-sensor-digitally-tracks-if-patients-have-ingested-their-medication.
5. Hatch AR. Digital mental health drug raises troubling questions [Internet]. 2018. Available from: https://www.phillyvoice.com/digital-mental-health-drug-cyborg-ethics-abilify-mycite
6. European Medicines Agency. Abilify MyCite: Withdrawal of the marketing authorisation application [Internet]. 2020. Available from: https://www.ema.europa.eu/en/medicines/human/withdrawn-applications/abilify-mycite
7. Kryzhanovska A. 6 reasons to build a health monitoring system for a hospital [Internet]. 2020. Available from: https://gearheart.io/blog/6-reasons-build-health-monitoring-system-hospital.
8. Propeller [Internet]. Available from: https://www.propellerhealth.com
9. Digital Therapeutic Alliance. Digital therapeutics: combining technology and evidence-based medicine to transform personalized patient care. Available from: https://dtxalliance.org/wp-content/uploads/2018/09/DTA-Report_DTx-Industry-Foundations.pdf
10. Sverdlov O, van Dam J, Hannesdottir K, Thornton-Wells T. Digital therapeutics: an integral component of digital innovation in drug development. Clin Pharmacol Ther 2018; 104: 72-80.
11. S3 connected health. Digital Therapeutics: pharma’s threat or opportunity [Internet]. Available from: https://www.s3connectedhealth.com/resources/white-papers/digital-therapeutics-pharmas-threat-or-opportunity
12. Food and Drug Administration. FDA permits marketing of first game-based digital therapeutic to improve attention function in children with ADHD. [Internet]. 2020. Available from: https://www.fda.gov/news-events/press-announcements/fda-permits-marketing-first-game-based-digital-therapeutic-improve-attention-function-children-adhd
13. Schutte-Rodin SL, Broch L, Buysee D, et al. Clinical guideline for the evaluation and management of chronic insomnia in adults. J Clin Sleep Med 2008; 4: 487-504.
14. Oleena [Internet]. Available from: https://oleena.com
15. National Institute for Health and Care Excellence (NICE). Evidence standards framework for digital health technologies: user guide [Internet]. Available from: https://www.nice.org.uk/Media/Default/About/what-we-do/our-programmes/evidence-standards-framework/user-guide.pdf
16. National Institute for Health and Care Excellence. Digital psychological therapy briefing – Deprexis for adults with depression [Internet]. 2018. Available from: https://www.nice.org.uk/Media/Default/About/what-we-do/NICE-advice/IAPT/iab-deprexis.pdf
17. National Institute for Health and Care Excellence (NICE). IAPT assessment briefing – Space from Depression for adults with depression [Internet]. 2018. Available from: https://www.nice.org.uk/Media/Default/About/what-we-do/NICE-advice/IAPT/IAB-space-from-depression.pdf
18. National Institute for Health and Care Excellence (NICE). BDD-NET for adults with body dysmorphic disorder [Internet]. 2019. Available from: https://www.nice.org.uk/Media/Default/About/what-we-do/NICE-advice/IAPT/iab-bdd-net-adults-body-dysmorphic-disorder-for-publication.pdf
19. Attuazione della Direttiva 93/42/CEE concernente i dispositivi medici. Decreto lgs. 24 febbraio 1997, n. 46 emendato col D. lgs. 25.01.2010, n.37 – Recepimento Direttiva 2007/47/CE [Internet]. Available from: http://www.salute.gov.it/imgs/C_17_pagineAree_1636_listaFile_itemName_1_file.pdf
20. Gazzetta Ufficiale dell’Unione Europea. Regolamento (UE) 2017/745 del Parlamento Europeo e del Consiglio [Internet]. Available from: https://eur-lex.europa.eu/legal-content/IT/TXT/?uri=CELEX%3A32017R0745
21. Food and Drug Administration. Software as a Medical Device (SaMD) [Internet]. 2018. Available from: https://www.fda.gov/medical-devices/digital-health/software-medical-device-samd
22. Chung J-Y. Digital therapeutics and clinical pharmacology. Transl Clin Pharmacol 2019; 27:6-11.
23. Kollins SH, DeLoss DJ, Cañadas E, et al. A novel digital intervention for actively reducing severity of paediatric ADHD (STARS-ADHD): a randomised controlled trial. Lancet Digit Health 2020; 2: E168-E178.
24. Endeavour TM. Instruction for use. Akili Interactive Labs 2020.
25. Gopal G, Suter-Crazzolara C, Toldo L, Eberhardt W. Digital transformation in healthcare – Architectures of present and future information technologies. Clin Chem Lab Med 2019; 57: 328-35.
26. Mobius MD. The status of mobile health apps: 11 facts [Internet]. 2019. Available from: https://www.mobius.md/blog/2019/07/the-status-of-mobile-health-apps-11-facts.



