Ornella Gonzato
Fondatrice e rappresentante legale Trust Paola Gonzato- Rete Sarcoma.Onlus
Tendenze Nuove, Numero 1 – 2022; 1-22: DOI: 10.32032/TENDENZENUOVE20220106.PDF

1. Introduzione
“Paziente esperto”, “patient advocate”, “caregiver”, “rappresentante dei pazienti”, “paziente individuale” sono espressioni che sottendono concetti e/o ruoli distinti, evidenziando nella terminologia, l’eterogeneità di quel gruppo di stakeholder, genericamente denominato “PAZIENTI”, che, includendo spesso anche le Organizzazioni di Pazienti, accorpa sotto un’unica etichetta una dimensione individuale e una collettiva assai più articolata.
Se per alcune delle espressioni sopra riportate, la definizione è semplice o pressoché intuitiva, per altre lo è un po’ meno, mancando univocità di significato/interpretazione. La conseguenza è una non chiarezza di ruoli e contesti, una difficoltà a specificare requisiti e risorse necessarie a svilupparne il ruolo adeguatamente, rendendo più confuso uno scenario a tutt’oggi in divenire.
Con dando di contribuire a far luce sul tema, e comprendere meglio le sue implicazioni sul piano pratico, si riportano di seguito alcuni dei tratti principali del contesto evolutivo – principalmente a livello europeo, statunitense e italiano – in cui si collocano due di esse – “paziente esperto” e “patient advocate”. Considerate le interdipendenze esistenti, vi saranno brevi cenni anche ad alcuni aspetti peculiari delle Organizzazioni di Pazienti, a cui tuttavia va riservata un’analisi approfondita che esula dalle nalità di questo lavoro.
Una ri essione nale su due espressioni aggiuntive – “patient engagement” e “patient involvement” -, centrali nel dibattito attuale e spesso utilizzate in modo intercambiabile, mira a evidenziare le interconnessioni concettuali e pratiche in un contesto di interazioni multi-stakeholder.
2. Il concetto di “paziente esperto”: dall’”expert patient” al “patient expert”
A livello internazionale non esiste una de nizione precisa e univoca di “paziente esperto” che, nella terminologia anglosassone, è formulato sia nei termini di “expert patient” sia di “patient expert”, espressioni non esattamente sovrapponibili.
“Expert patient”, de nizione creata nel 1985 da Tuckett, qualifica come “expert” il paziente “in quanto paziente con esperienza della propria malattia (illness)”. Secondo questa prospettiva, l’interazione tra medico e paziente si realizza nell’incontro -alla pari e con ruoli distinti- tra due “esperti”: da un lato il paziente, forte dell’esperienza del vivere con la malattia (illness), dall’altro il medico, esperto della patologia (disease)(1,2).
‘‘Expert patient’’ compare ufficialmente in un documento – ‘The Expert Patient: a new approach to chronic disease management in the 21st century’- che, muovendo dall’analisi dei problemi della cronicità in Gran Bretagna, fornisce un insieme di raccomandazioni per un nuovo approccio alla gestio- ne delle patologie croniche(3). Il documento prodotto dal Departement of Health (DoH), a seguito della pubblicazione nel 1999 del report “White Paper, Saving Lives: Our Healthier Nation”(4), viene approvato dal Parlamento britannico nel 2001 e diventa parte integrante della programmazione del National Health Service (NHS). Le raccomandazioni contenute mirano allo sviluppo di attività per incoraggiare e supportare i pazienti af nchè possano svolgere un ruolo attivo nel proprio percorso di cura. L’adozione e l’implementazione di “Programmi di formazione/educazione- Expert Patient Programmes/ Patient self-management Programmes – da parte del NHS ne costituiscono lo strumento operativo. Educare/istruire i pazienti sulla propria patologia (therapeutic education) ma anche sviluppare motivazione e consapevolezza affinché possano utilizzare le proprie esperienze e conoscenze per un controllo attivo (self-management) sulla malattia sono tra i principali obiettivi formativi. Ad essi si aggiunge anche l’opportunità d’informare meglio i professionisti per costruire programmi di co-gestione con i pazienti(5,6).
Il concetto di “expert patient” che si sviluppa nel contesto della cronicità, origina fondamentalmente da due considerazioni:
1. i pazienti con patologia cronica hanno un’esperienza/conoscenza della malattia (illness) che nessun professionista può avere, poiché sperimentano quotidianamente le difficoltà sulla propria vita;
2. l’esperienza e la conoscenza del vivere con la malattia (illness) costituisce una risorsa non utilizzata che, qualora impiegata, potrebbe apportare bene cio sia ai pazienti, sia al sistema sanitario, sempre più gravato dal carico gestionale e nanziario di tali patologie.
“Expert patient” in questo contesto diviene chi possiede esperienza della malattia (illness) e conoscenza della patologia (disease) tali da poter giocare un ruolo centrale nella sua gestione, contenendone l’impatto negativo nella vita quotidiana(7,8).
“Patient expert”, in cui “patient” quali ca il sostantivo “expert”, trova, in Europa, il principale fondamento nei documenti dell’Agenzia Europea del Farmaco (EMA) riguardanti il percorso, avviato nel 1995 e rafforzatosi nel 2006 con l’istituzione del “Patients and Consumers Working Party (PWCP)”, per lo sviluppo e la gestione delle interazioni con i propri stakeholder. Tra questi documenti, si richiamano sinteticamente i seguenti:
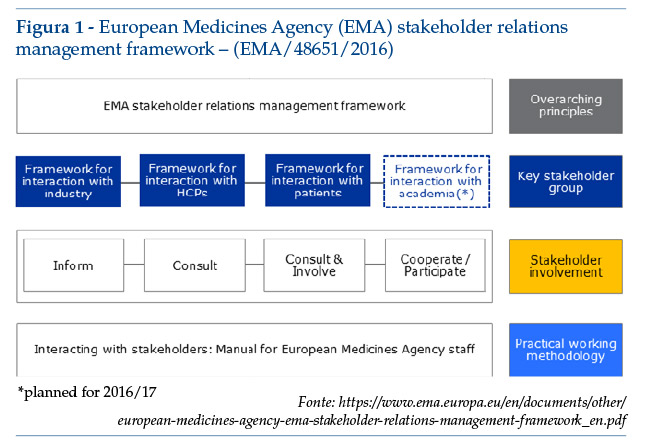
1.“European Medicines Agency (EMA) stakeholder relations management framework – (EMA/48651/2016)” documento aggiornato nel 2016 che stabilisce i principi per strutturare e gestire le interazioni (rapporti/relazioni) tra l’Agenzia e i propri stakeholder, individuati preliminarmente nelle “associazioni”, “organizzazioni” e “parti” aventi interesse e/o sulle quali l’attività dell’Agenzia possa avere un impatto signi cativo. La volontà politica sottostante al documento è quella di promuovere e sviluppare una metodologia appropriata per interagire con le quattro tipologie di stakeholder – identificate nei professionisti sanitari, accademia, industria farmaceutica e pazienti- su temi relativi alla valutazione e all’autorizzazione dei farmaci, ottemperando a quanto stabilito dall’art 78 del Reg. EU 726/2004(9). Al ne di ottimizzare la gestione delle interazioni con ciascun stakeholder, sono identificati i seguenti quattro livelli di coinvolgimento (involvement): informazione, consultazione, consultazione e coinvolgimento attivo, cooperazione/partecipazione (figura 1). Livelli diversi implicano differenti gradi d’impegno e di responsabilità tra le Parti(10).
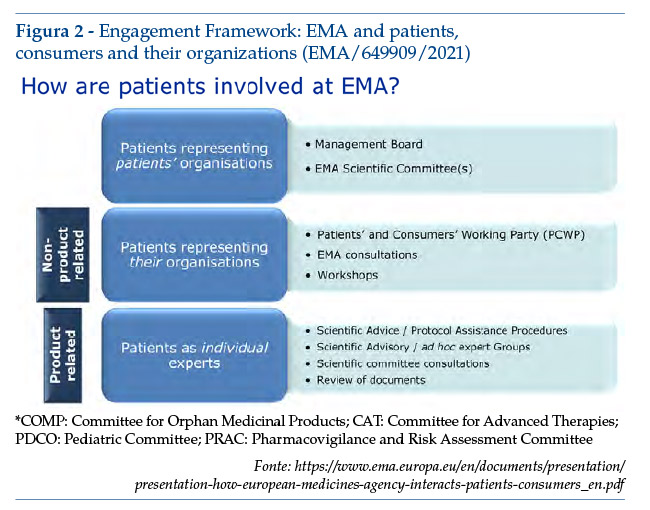
2. “Engagement Framework: EMA and patients, consumers and their organizations” (EMA/649909/2021), documento del 2022 che, collegandosi al precedente, stabilisce obiettivi e metodologie per gestire le interazioni tra EMA e il Gruppo di stakeholder costituito da “Pazienti, consumatori e loro organizzazioni”(11). Esso include:
• organizzazioni di pazienti;
• organizzazioni di consumatori;
• pazienti o familiari (carers), ovvero persone con esperienza di cosa
signi chi vivere con una specifica condizione di salute/malattia.
A seconda della natura/tipologia delle attività previste, le interazioni
possono richiedere la presenza di:
• pazienti membri di Comitati Scientifici EMA (COMP, CAT, PDCO, PRAC*) in rappresentanza di tali Comitati;
• pazienti in qualità di rappresentanti dell’Organizzazione di appartenenza;
• pazienti (non necessariamente afferenti a un’Organizzazione di Pazienti) in qualità di “esperti individuali” (“patients as individual experts”). Considerata la gamma di attività svolte dall’Agenzia, e la loro diversa natura, il previsto coinvolgimento dei pazienti può estendersi dall’inclusione nella composizione del Board di Direzione e di Comitati Scientifici dell’Agenzia, alla partecipazione a conferenze e workshops, al contributo nei processi di valutazione e autorizzazione di un farmaco fino al coinvolgimento nella stesura di linee guida. Entrando nel merito della tipologia di attività in cui “pazienti quali esperti individuali” possono essere coinvolti, emerge che si tratta di attività “prodotto speci che”, ovvero relative al processo di valutazione di uno specifico prodotto medicinale – come, ad esempio, procedure di Scienti c/Protocol Advice e di revisione della documentazione(12)(figura 2).
Coinvolgere “pazienti quali esperti individuali” a questo livello ha lo scopo di includere la prospettiva di chi, avendo esperienza diretta della malattia e della sua gestione nella quotidianità, può fornire input utili, a titolo personale, per la valutazione di un farmaco e per un suo utilizzo il più possibile appropriato e sicuro. Un database raccoglie i nominativi, attingendo a più fonti, incluse le Organizzazioni di Pazienti eleggibili a cui viene richiesta indicazione oltre alla registrazione diretta di qualsiasi paziente, a prescindere dalla sua appartenenza ad un’Organizzazione di Pazienti (“Register as patient expert”)(13,14). A tal proposito, il documento “Stakeholders and Communication Division EMA individual experts’ stakeholder database: patients and consumers- Frequently asked questions” chiarisce che “the Agency’s first port of call when looking for patients is via their list of registered eligible patients’ and consumers’ organisations.”(15), esplicitando, in tal modo, il ruolo assegnato alle Organizzazioni di Pazienti. In aggiunta, specifica che pazienti e caregiver sono invitati a registrarsi direttamente, riconoscendo che il loro potenziale contributo si fonda sull’esperienza di vita reale e non necessita di background nell’area medica o regolatoria. Il supporto informativo/educazionale strumentale alla loro partecipazione alle attività stabilite compete a EMA (“Is anyone able to be part of the database? Yes, patients, carers and consumers are all invited to register in the individual experts’ stakeholder database. Is a background in medicine or regulatory affairs necessary? Patients and consumers are invited because they can contribute valuable information based on their real-life EXPERIENCES. A background in medicine or regulatory affairs is not necessary. EMA provides support and educational material to prepare patients and consumers invited to the Agency to participate in an activity”).
Il database dei pazienti, assieme a quello con i nominativi delle Organizzazioni di Pazienti, che hanno soddisfatto i requisiti di eleggibilità fissati da EMA, costituisce il network di riferimento per le attività dell’Agenzia.
3. Patients and Healthcare Professionals Training strategy for patients and consumers involved in EMA activities (EMA/664931/2014 Rev. 1), documento del 2014 che definisce la strategia dell’EMA per la formazione/training di due specifici gruppi di stakeholder, quello dei “Pazienti” e quello dei “Professionisti Sanitari”(16). Con riferimento al gruppo dei Pazienti, e con la nalità di ottimizzare tutti i possibili contributi, EMA offre e supporta programmi di formazione/training differenziando – come esplicitato nel documento- contenuti e modalità (video, webinar, seminari, informative, ecc) in relazione ai diversi soggetti coinvolti e alle attività previste.
Lo sviluppo di competenze (capacity building), si con gura pertantostrumentale per un effettivo coinvolgimento/partecipazione ai processi regolatori relativi ai farmaci, così come evidenziato anche nel documento EMA del 2022 sopra citato. (Capacity-building: To optimise their contribu- tion, EMA provides patients with a training programme to help them under- stand the Agency’s mandate as well as their expected role in the medicine’s regulatory process. The training provided is tailored and based on the parti- cular activity where the patient will participate and is complemented by personalised and one-to-one support. Some patients’ organisations or collaborative projects have also developed training to empower patients to play a recognised advocacy role at European level- Engagement Framework: EMA and patients, consumers and their organizations – EMA/649909/2021).
Alla luce di quanto descritto, si osserva che il concetto di “paziente esperto (expert patient)” pur rimanendo centrato su “chi possiede esperienza di cosa signi chi vivere con una speci ca condizione di malattia” tende ad assumere, attraverso lo sviluppo di “capacity building”, in una precisa area di competenza -in questo caso, quella regolatoria del farmaco- una valenza ulteriore che sembra estenderne il significato.
“Patient expert” è la definizione utilizzata anche da EUPATI (European Patients’ Academy on Therapeutic Innovation) in seno al progetto formativo/educativo avviato con IMI (Innovative Medicines Initiative) nel 2012, finalizzato a sviluppare conoscenze e competenze idonee per un coinvolgimento attivo (engagement) dei pazienti lungo l’intero ciclo di vita di un farmaco, dalla fase di ricerca e sviluppo alle fasi di sperimentazione non-clinica e clinica, dai processi regolatori per l’autorizzazione alla farmacovigilanza e all’Health Technology Assessment (HTA)(17,18). Il programma formativo non focalizza su alcuna speci ca malattia o area terapeutica; al contrario, è centrato su processi, attività, procedure e metodologie comuni allo sviluppo di qualsiasi tipo di farmaco e sul contributo/coinvolgimento (engagement) dei pazienti nelle diverse fasi di processo. L’offerta educazionale EU- PATI-IMI attraverso “Programmi di training per pazienti esperti –EUPATI Patient Expert Training – è rivolta principalmente a pazienti e loro rappresentanti (quali caregiver, persone che operano nelle Organizzazioni Pazienti); tuttavia è aperta anche a chiunque (cittadino) possa esser interessato. A completamento del training, EUPATI rilascia un certi cato che, testualmente, “offre l’opportunità di essere riconosciuti come expert patients”. (“Graduates of the EUPATI Patient Expert Programme are also known as EUPATI Fellows. The EUPATI Fellow title certi es the knowledge gained and gives graduates the opportunity to be recognised as expert patients”)(19,20).
Riconoscendo ancora una volta che la formazione è fondamentale per un coinvolgimento attivo in processi che richiedono conoscenze/competenze tecniche a monte, val la pena di notare che nel contesto “EUPATI Patient Expert Training” i termini “patient expert” e “expert patient” sono utilizza- ti in modo intercambiabile, con il rischio di ingenerare confusione. La certiFIcazione inoltre offre l’opportunità di esser riconosciuti come “expert patient” a “pazienti e loro rappresentanti”, target principale dell’azione formativa, e a chiunque sia interessato.
La terminologia “patient expert” è adottata anche in un recentissimo documento (2021) che riguarda il coinvolgimento (involvement) dei pazienti nel contesto della ricerca oncologica – Principles of successful Patient involvement in CANCER research (Berlin Declaration- EU against cancer – Initiative of the Trio Presidency of the EU council Germany, Portugal, Slovenia– in cui si sottolinea la necessità di considerare sempre attentamente l’ETEROGENEITÀ interna al gruppo di stakeholder identificato genericamente come “PAZIENTI”(21). Nel dettaglio, il documento mette in guardia sulle differenze concettuali tra i diversi attori (“With regard to the group of patients, we must acknowledge the conceptual differences between individual patients and their carers, patient advocates, patient organization representatives and patient experts as well as their varying impact and expertise”), per i quali fornisce utili definizioni, distinguendo tra:
• “Pazienti individuali”, pazienti con esperienza diretta del vivere con una malattia e capaci per questo di portare/offrire la propria esperienza soggettiva (“individual patients means individuals with personal experience of living with a condition, who can share their subjective experience”).
• “Caregiver” chi fornisce supporto al paziente individuale (“persons who support individual patients”).
• “Patient advocates” coloro che hanno capacità di visione ed esperien- za tali da supportare una comunità di pazienti affetti da una speci ca malat- tia. Possono esser af liati o meno a un’organizzazione (“persons who have the insight and experience in supporting a larger population of patients living with a speci c condition. They may or not may be af liated with an organization”).
• “Patient experts” coloro che, in aggiunta alla conoscenza della pato- logia (disease), possiedono/hanno acquisito “conoscenze tecniche” relative ai processi di Ricerca e Sviluppo (R&D) e/o dell’area regolatoria. (“peoplewho, in addition to disease-speci c expertise, have the technical knowledge in R&D and/or regulatory affairs”).
• “Rappresentanti di Organizzazioni Pazienti” coloro che hanno ti- tolo a rappresentare ed esprimere la prospettiva/ visione collettiva di un’organizzazione pazienti su temi inerenti la patologia d’interesse (“per- sons who are mandated to represent and express the collective views of a pa- tient organization on a speci c issue or disease area”).
Il documento evidenzia che, sebbene la pluralità di prospettive possa costituire sempre una ricchezza, per ottimizzare i contributi è fondamentale identificare precisamente “CHI” coinvolgere, in relazione a speci che finalità e livelli di intervento, in un range che va dal “paziente individuale” privo di qualsiasi formazione al “patient advocate”, al “patient expert”. Ne consegue la necessità di una chiara de nizione dei requisiti, in termini di conoscenze/esperienze/competenze e/o di ruoli necessari.
3. Il concetto di “patient advocate”: confronto e differenze rispetto al “patient expert”
“Patient expert” non coincide con “patient advocate”; il secondo, tuttavia, spesso include il primo.
Il termine “advocacy” deriva dal latino “ad vocare” letteralmente “chiamare a sé; chiamare in aiuto qualcuno”. Nonostante le molteplici de nizioni e modelli sviluppatisi nel tempo, a partire dagli anni ’70, quando l’attività di advocacy costituiva parte integrante della professione infermieristica, vi è consenso generale nel considerare che il concetto di “advocacy” implichi sempre il coinvolgimento di “una persona che rappresenta un’altra/ una persona che chiede/perora per conto di un’altra” e più precisamente “agisce per conto di chi è vulnerabile e lo richiede”(22-26). Ne deriva che chiunque abbia interesse può svolgere attività di “advocacy” a bene cio di un paziente: dagli infermieri ai clinici ai familiari o anche altre gure. Negli Stati Uniti, ad esempio, il National Cancer Institute (NCI) definisce “patient advocate” chi guida un paziente nel proprio percorso di cura attraverso i servizi sanitari. Si tratta di un ruolo ricoperto da una gura non sanitaria che, a seguito di formazione appropriata, è capace di favorire la comunicazione tra paziente e professionisti, di fornire informazioni sulla malattia, di supportare il paziente nello svolgimento di un insieme di attività – amministrative, organizzative e assicurative. Il NCI specifica, inoltre, che “patient advocate” può esser definito anche come “patient navigator”(27,28).
A prescindere da quest’ultima de nizione, e riprendendo il concetto di “advocacy” sopra illustrato, val la pena considerare che se nessuno nega che i professionisti sanitari agiscano come “advocates” per i propri pazienti, nessuno può neanche negare che vi siano aspetti dell’”advocacy” in cui i pazienti/loro gruppi possono apportare un contributo diretto importante, fornendo una prospettiva unica, quella del vivere con una patologia/condizione di salute, che nessuna altra Parte possiede. Qui emerge anche la differenza sostanziale tra il concetto di “health advocacy”, come azione esercitata non direttamente da pazienti e finalizzata ad apportare bene cio a livello del singolo, e quello moderno di “patient advocacy”, in cui sono i pazienti/ loro grup- pi e rappresentanti ad agire, far sentire la propria “voce”, per cercare soluzio- ni capaci di consentire/migliorare l’accesso ai trattamenti a bene cio della co- munità di riferimento. In maniera simile, seppur non sovrapponibile, il con- cetto di “patient-centred” è distinto da quello di “patient-centric”/“patient- led”/“patient-driven”, indicando attività- ma anche organizzazioni- “guidate” dai bisogni e preferenze dei pazienti nel primo caso e attività “a guida” di pazienti/caregiver nel secondo(29,30,31).
Le origini della moderna “patient advocacy” risalgono all’azione svolta dalla comunità dei pazienti con HIV che, alla ne degli anni ‘80, ha generato un cambiamento dello “status quo”, non solo dando visibilità ai bisogni di questi pazienti, ma in uendo direttamente sull’agenda politica in tema di sviluppo e accesso ai farmaci e ai trattamenti necessari(32). “Making the difference – Agire per fare la differenza” esprime oggi sinteticamente la visione strategica delle Organizzazioni di Patient Advocates che agiscono per in uire sulle decisioni a livello politico-istituzionale- e a tutti i livelli necessari- allo scopo di ridurre iniquità d’accesso a farmaci e trattamenti, assicurando il rispetto dei diritti dei pazienti con una specifica patologia/ condizione di salute. In altri termini esercitano un’azione di lobbying, in uendo sull’agenda politica in tutte le aree di interesse per migliorare esiti/condizioni di salute per una determinata patologia, intervenendo in tutti gli ambiti necessari, dalla ricerca all’accesso ai farmaci, all’organizzazione dei servizi /prestazioni(33).
Tre sono i principi che guidano la moderna “patient advocacy”: rappresentanza, mobilitazione, empowerment. Quest’ultimo definito, nella sua dimensione collettiva, come “processo multidimensionale attraverso cui gruppi/ comunità sono in grado di esprimere i propri bisogni, esplicitare le difficoltà/ preoccupazioni, consigliare strategie di miglioramento per un coinvolgimento nei processi decisionali ed esercitare un’azione a livello politico, sociale, culturale per rispondere a quei bisogni”, coglie e sintetizza l’essenza dell’advocacy(30). Si delinea pertanto uno spazio d’intervento più ampio e un ruolo diverso rispetto a quello attribuito a un’azione di “advocacy” spesso descritta semplicemente come “attività di sensibilizzazione dell’opinione pubblica e delle istituzioni relativamente a un determinato gruppo di patologie/pazienti”. Alcuni Autori identificano anzi quest’ultima tipologia di attività come una delle fasi – solitamente iniziale – del percorso evolutivo di un’azione di “advocacy” matura e moderna, il cui obiettivo è in uire a tutti i livelli decisionali necessari, ponendosi come partner in un contesto d’interazione ef cace tra differenti stakeholder, per trovare assieme soluzioni/risposte adeguate(34). E un raggio d’azione che va oltre l’”attivismo” per diventare “partnership”.
L’acquisizione di conoscenze e lo sviluppo di competenze nelle diver- se possibili aree d’intervento (ricerca, organizzazione dell’assistenza, accesso ai farmaci ma anche comunicazione, negoziazione, ecc.) si configurano ancora una volta strumentali all’efficacia dell’azione di advocacy.
Una definizione di “patient advocate” si ritrova anche nel recente Glossario della Food&Drug Administration- FDA “Patient-Focused Drug Development Glossary Standardized nomenclature and terminologies related to patient-focused medical product development (2018)(35). Il documento, che accompagna le Guide elaborate in seno al Patient-focused drug development (PFDD)- Programma FDA sviluppato in accordo con il “21st Century Cures Act and the FDA Reauthorization Act of 2017”(36), con l’obiettivo di “incorporare” la voce dei pazienti nello sviluppo e valutazione dei farmaci, riporta le seguenti definizioni:
• Patient advocate: Persona o Gruppo di persone che possono o meno far parte di una speci ca popolazione/comunità pazienti, che ha/ hanno un ruolo nel promuovere una causa influendo sulle politiche a bene cio della salute dei pazienti cui si riferiscono.
Nel glossario compaiono anche le definizioni di “patient”, “patient representative” e, per la prima volta, quella di “patient partner”, come di seguito riportato. È invece assente la definizione di “patient expert”.
• “Patient: Any individual with or at risk of a specific health condition, whether or not he or she currently receives any therapy to prevent or treat that condition. Patients are the individuals who directly experience the benefits and harms associated with medical products”.
• “Patient representative: An individual, who may or may not be part of the target population, who has direct experience with a disease or condition (e.g., a patient or caregiver) and can provide information about a patient’s experience with the disease or condition”.
• “Patient partner: An individual patient, caregiver or patient advocacy group that engages other stakeholders to ensure the patients’ wants, needs and preferences are represented in activities related to medical product development and evaluation”.
In Europa, anche EMA ha elaborato un recentissimo documento che, muovendo dalla necessità di includere la prospettiva dei “pazienti”, sia nei processi regolatori di valutazione di un farmaco sia in quelli del suo sviluppo industriale, pone le basi per lo sviluppo di successive Linee Guida ICH. La finalità è quella di de nire un approccio metodologico robusto e armonizzato, capace di strutturare gli input /contributi forniti dai pazienti per informare al meglio i processi decisionali a diversi livelli, incluso quello della valutazione economica delle tecnologie (HTA). Il documento non è accompagnato da un glossario; fa riferimento genericamente a “pazienti e loro caregiver quali partner” di autorità regolatorie e di produttori farmaceutici; tuttavia, evidenzia che il crescente sviluppo di azioni di “advocacy e engagement” dei pazienti ha generato un contesto ricco, ma ancora complesso a cui far riferimento per incorporare la prospettiva dei pazienti, rendendo così più che mai critico lo sviluppo di un approccio metodologico armonizzato (“Growing patient advocacy and patient engagement, and continued advances in communication technologies, internet, social media, and a proliferation of information services and sources, have created a rich yet complex environment for eliciting and incorporating patient perspectives throughout the drug development process.”(37). Il documento evidenzia tuttavia in premessa che “i pazienti sono esperti del vivere con la malattia…conoscono l’impatto della malattia nella propria vita… apportano una prospettiva unica che nessun esperto clinico, scienti co o altro può fornire” (“Patients have direct experience in living with a disease. They have rsthand knowledge of the impact of the disease on their life and on how they feel and function. They bring unique and valuable perspectives to drug development that cannot be provided by the clinical, scientific, legal and other experts”). Merita sottolineare che questa de nizione coincide essenzialmente con quella riportata dalla Dichiarazione di Berlino nei termini di “pazienti individuali (individual patients)” nonché con quella di “pazienti quali esperti individuali (patients AS individual experts)” di EMA, nendo, in ultima analisi, per equivalere alla definizione di “expert patient” formulata, in origine, da Tuckett.
In Italia, la complessità del contesto, emerge anche dal nuovo Codice Deontologico di Farmindustria del 2022, che, nella sezione relativa ai rapporti tra aziende farmaceutiche e pazienti/loro organizzazioni, inserisce anche i “pazienti esperti” (“Rapporti tra le Aziende Farmaceutiche, le Associazioni dei Pazienti e i Pazienti esperti”), quali “pazienti che, oltre ad avere conoscenza diretta della patologia, sono dotati di specifica competenza ed esperienza in aspetti connessi alla ricerca e sviluppo dei farmaci, alle attività regolatorie o in attività di advocacy intesa quale capacità di promuovere e supportare le cause e le necessità di una pluralità di pazienti”(38). In aggiunta, si specifica che le competenze “dovranno essere effettive e documentabili e potranno essere corredate da certificazioni o attestati rilasciati a seguito di partecipazione a corsi e programmi formativi realizzati da terze parti quali cate ed indipendenti.”. Ai “pazienti esperti” così identificati, “previa applicazione di uno specifico processo approvativo segregato” è consentito il coinvolgimento quali “consulenti per servizi come partecipazione ad advisory board e relatori”. È interessante evidenziare, in merito ai requisiti di “competenza ed esperienza”, l’equiparazione tra aspetti inerenti l’ambito regolatorio di sviluppo del farmaco e attività di advocacy, che, come precedentemente illustrato e qui ribadito, ha un campo d’azione che si estende oltre l’area del farmaco, nell’interesse di una pluralità.
Alla luce del quadro sin qui delineato, alcune riflessioni sono d’obbligo:
• ogni paziente è individualmente esperto della propria condizione di malattia (individual patient/ patient AS individual expert/ expert patient), o meglio del vivere con la propria malattia (illness), anche quando può non essere capace di analizzare la propria esperienza, di descriverla con strumenti “oggettivi” o di discuterne o di volerne discutere in contesti più “complessi” che non siano ad esempio quelli della narrazione tra pari;
• ogni paziente, come sopra definito, può portare/offrire la propria esperienza/prospettiva a titolo personale/individuale, a prescindere dall’aver ricevuto una formazione in speci che aree di competenza;
• “patient expert”, diversamente da “patient advocate” che indica un ruolo, costituisce un prerequisito per un coinvolgimento attivo del paziente – ma anche di chiunque altro sia interessato, perlomeno nel contesto “EU- PATI Patient Expert Training” (“While the programme is mainly addressed to patients and patient representatives — e.g., carers and persons working for patient organization –, it is open to ALL individuals interested in medicines R&D and patient engagement”) – a diversi livelli e lungo uno spettro di attività distinte tra loro. La definizione di “patient expert” fa essenzialmente riferimento all’acquisizione di specifiche “conoscenze/competenze”, differenziate e diversificate in relazione ai diversi ambiti di applicazione;
• la formazione – formale, informale o non formale-, e più in generale, lo sviluppo di “capacity building” in specifiche aree – siano esse relative alla patologia (therapeutic education) e/o a processi riguardanti l’accesso a farmaci, all’organizzazione dell’assistenza, nonché alla comunicazione e capacità d’impatto- si configura come strumentale all’efficacia ed efficienza delle interazioni multi-stakeholder;
• programmi di formazione/educazione sono funzionali all’ottimizzazione dei contributi che i pazienti possono apportare, sia a livello individuale/soggettivo sia a livello di gruppi/organizzazioni rappresentanti la comunità di riferimento. Se nel secondo caso è chiara la valenza a beneficio della popolazione rappresentata, nel primo caso val la pena distinguere due livelli: utilità per se stessi (self-management) in seno al proprio percorso di cura, e contributo, a titolo personale/individuale, a processi con ricaduta sulla comunità dei pazienti interessati;
• programmi formativi/educazionali sono necessari anche per i professionisti, per sviluppare un approccio culturale capace di includere la prospettiva dei pazienti, di riconoscerli quali partner di sistema, in un insieme di processi e attività, percorsi da condividere fin dall’inizio, fin dalla fase di progettazione.
4.”Patient engagement” e “patient involvement”
“Come” includere i contributi di un gruppo eterogeneo di stakeholder come quello dei “PAZIENTI” rimane una questione centrale sul piano pratico. Tuttavia, prima del “come”, sarebbe indispensabile individuare sempre esattamente “CHI” all’interno del gruppo, coinvolgere – precisandone requisiti di esperienza, conoscenza e competenza – dopo aver stabilito, con chiarezza, quali le finalità e le aree d’intervento (“perché” e “cosa”).
Merita, a questo punto, focalizzare l’attenzione anche sulla terminologia utilizzata per de nire il tipo d’interazione tra i differenti stakeholder(39,40). “Involvement” e “engagement” (tradotti nella lingua italiana principalmente come “coinvolgimento”, “coinvolgimento attivo”, “partecipazione”) rappresentano concetti distinti, anche se spesso usati in maniera intercambiabile e/o con significato diverso nei diversi contesti e livelli di applicazione (regolatorio, clinico-assistenziale, ricerca, politiche sanitarie) e di dimensione (individuale o organizzativa).
L’FDA definisce “Patient engagement” l’insieme di “attività in cui i pazienti, in qualità di stakeholder, vengono coinvolti con la nalità di condividere le proprie esperienze, prospettive, bisogni e supportare in tal modo, l’FDA nella propria mission”(35).
Nel contesto regolatorio europeo, “engagement “è il termine per denominare in senso ampio l’interazione/ la relazione (la natura relazionale, sistemica e strategica) con i propri stakeholder, mentre “involvement” viene utilizzato come termine ombrello, con riferimento al “coinvolgimento” operativo degli stakeholder ai differenti livelli necessari per raggiungere gli obiettivi strategici. Come riportato inizialmente, quattro sono i livelli di involvement individuati – informazione, consultazione, consultazione e coinvolgimento, cooperazione/partecipazione- che costituiscono le basi metodologiche dell’operatività dell’EMA nell’interazione (engagement) con i propri stakeholder.
In Italia, il Documento di Consenso sul “Patient engagement”(41), elaborato nel 2017, relativo speci catamente all’ambito clinico-assistenziale della cronicità, mantiene il termine inglese “engagement” per “meglio dialogare con la letteratura scientifica di riferimento e con i documenti di indirizzo, insistendo – allo stesso tempo – sull’importanza di adottarne una traduzione italiana nel contesto clinico- assistenziale di educazione, comunicazione e relazione con la persona con patologia cronica. In tale direzione, opzioni di traduzione come “coinvolgimento attivo”, “protagonismo della persona nel percorso di as- sistenza e cura”, “co-autorialità nel percorso sociosanitario” e metafore come “diventare co-piloti e non soltanto passeggeri nel percorso sanitario” sembrano potenzialmente ben esprimere la complessità del concetto di engagement”. La dicitura “engagement” non è però più accompagnata dalla qualifica “patient”, “al ne di sottolineare la natura relazionale-sistemica del termine engagement che mette in gioco (su un piano fattuale e simbolico, per la natura stessa del concetto) diversi attori e diversi contesti di vita, di assistenza e di cura… Nell’ambito clinico-assistenziale della cronicità, engagement pertanto è un concetto sistemico… L’engagement nell’ambito clinico assistenziale della cronicità è un concetto-ombrello che ne articola, sistematizza e include altri, quali adherence, compliance, empowerment, activation, health literacy, shared decision making, activation. L’engagement è funzione della capacità, della volontà e della scelta graduale delle persone di assumere un ruolo proattivo nella gestione della propria salute”. Nel glossario allegato al documento, viene messa anche a confronto la differenza/relazione concettuale tra la definizione di “paziente esperto” con “patient engagement”, sottolineando che il primo è strumentale al secondo: “la definizione di paziente esperto denota le abilità e le conoscenze del paziente in merito alla sua malattia e al vissuto psicologico con essa. Il paziente esperto è il presupposto e non il risultato di un engagement efficace e funzionale alla crescita di un modo diverso di curarsi/curare, governando il processo di cura stesso”. Chiarire la natura sistemica e la molteplicità di livelli –individuale, interpersonale, organizzativo, socio-comanitario e politico/istituzionale– consente di individuare chi è coinvolto nella relazione- ovvero pazienti, caregiver, professionisti sanitari e team assistenziale in primis- e quindi affrontare la questione centrale del come, ovvero con quali metodologie e strumenti, realizzare l’engagement. Tra questi, la formazione/educazione su specifici temi (cosa) costituisce l’asse portante per tutti gli attori, coerentemente ai ruoli: programmi di educazione terapeutica assistenziale e “peer education” assieme a interventi di counselling psicologico per aumentare motivazione auto-consapevolezza, per i pazienti e i caregiver; “conoscenze e competenze specifiche di promozione dell’engagement nella pratica clinica quotidiana”, per i professionisti e il team assistenziale. A tutto ciò si aggiunge la necessità di formazione per le Organizzazioni di Pazienti af nché sostengano e promuovano – in una logica di “ecosistema” – la cultura dell’engagement a beneficio dei pazienti.” Le associazioni di persone con patologia cronica, di caregiver e di volontari costituiscono una fonte inestimabile di educazione, supporto informativo, pratico e soprattutto emotivo per le persone e le loro famiglie”.
Nell’ambito della ricerca, il National Institute for Health and Care Research (NIHR) ha elaborato una guida rivolta ai ricercatori e a chiunque abbia interesse a coinvolgere il pubblico (inteso quale insieme di pazienti, pazienti potenziali, caregiver, utenti di servizi, cittadini), – Briefing notes for researchers – public involvement in NHS, health and social care research(42)– distinguendo tra:
• “involvement”: quando la ricerca non è “sui” o “per” i pazienti ma “con” i pazienti. Indica un rapporto di coinvolgimento attivo tra le parti in qualità di partner nel co-progettare e co-sviluppare la ricerca;
• “engagement”: quando l’attività riguarda la disseminazione dell’informazione e della conoscenza sulla ricerca al pubblico;
• “participation”: quando i pazienti prendono parte a studi, ovvero sono soggetti su cui gli studi sono condotti.
“Involvement” è il termine utilizzato anche dal Regolamento (UE) n. 536/2014 sulla sperimentazione clinica di medicinali per uso umano. L’All 1, lettera D-17 e), relativo al Protocollo di studio, stabilisce che: “nel caso in cui i pazienti siano coinvolti nel disegno della sperimentazione clinica, è necessa- ria una descrizione del loro coinvolgimento (“where patients were involved in the design of the clinical trial, a description of their involvement”)(43).
Il coinvolgimento attivo (involvement) nella ricerca non è una rivoluzione ma piuttosto un’evoluzione del contesto nel suo insieme. Lo sviluppo di conoscenze, attraverso programmi formativi/educativi e l’implementazione di esperienze sul campo costituiscono un processo di apprendimento continuo, di “learning by doing” con potenzialità generatrice nuova, sia per i pazienti che per i professionisti, in seno a partnership effettive e non solo formali. “Involvement” nella ricerca non riguarda solo le diverse fasi della ricerca clinica ma l’intero processo, in un “continuum” che si estende dalla ricerca di base a quella traslazionale fino a quella clinica. Numerosi sono gli esempi di questo “coinvolgimento attivo” dei pazienti, o più correttamente delle Organizzazioni di Pazienti che in alcuni casi – in particolare nell’area della rarità – va oltre l’involvement diventando azione capace di indirizzare e guidare la ricerca (“research patient driven”)(44,45).
Vale la pena richiamare, a questo punto, l’art. 72 del Reg EU 536/2014 relativo alla “co-sponsorizzazione”, che stabilisce che “una sperimentazione clinica può avere uno o più promotori”, lasciando aperta la possibilità che uno di questi possa essere costituito anche da “Pazienti”(40). In aggiunta, rilevante in questa prospettiva, è anche il framework sviluppato dall’EMA (STAMP) per supportare- nell’area degli “unmet needs” – Organizzazioni non-profit (definite “champion”) che abbiano interesse ma non possiedano competenze sufficienti per avviare processi di “drug repurposing”(46).
In generale, le strategie e il livello di “involvement” dei pazienti nella ricerca dovrebbero dipendere da un insieme di fattori, a iniziare dalla natura dei quesiti oggetto di ricerca fino alla chiara definizione dei rapporti, ruoli e relativo potere decisionale degli attori coinvolti. A tal proposito, la Dichiarazione di Berlino specifica: “Depending on the specific research question to be addressed, the goals and resulting involvement strategies may differ widely. In some cases, a pragmatic, outcome-oriented or more “top-down” approach may suf ce while in others a democratic, rights-based or more “bottom-up” approach may be the better choice. In any case, it should be decided and made clear from the beginning who leads a project, which level of involvement is appropriate, or how decision-making power will be shared between partners. For certain projects, it may be suf cient to solely consult the persons or organizations involved. However, tokenism, mere afterthought or tick-box exercises must be avoided. In other cases, higher levels of involvement are justi ed, manifesting as genuine collaboration, co-creation or even putting “patients in the driver’s seat”, i.e. giving patients control over the research process. Patient-led or patient-driven research activities should be strengthened and supported wherever possible. In general, higher levels of patient involvement require increasing opportunity to impact on and co-shape research in order to create added value”.
Per completezza, merita, infine, fare un minimo cenno ai termini e concetti di “coinvolgimento” e “partecipazione” utilizzati nel quadro normativo italiano, riferiti specificatamente non a singoli individui ma a Enti.
“Coinvolgimento attivo” è il termine utilizzato nel Codice del Terzo Settore (D.Lgs117/2017), che, all’art. 55, specifica: “le amministrazioni pubbliche, nell’esercizio delle proprie funzioni di programmazione e organizzazione a livello territoriale degli interventi e dei servizi.., assicurano il coinvolgimento attivo degli Enti del Terzo Settore, attraverso forme di co-programmazione e co-progettazione e accreditamento…”(47).
Sempre con riferimento non a singoli individui ma a Organizzazioni di Pazienti, il “coinvolgimento attivo”, distinto dall’”attivismo civico” che ne costituisce tuttavia la base evolutiva, trova spazio significativo nel quadro normativo dell’area oncologica («Rev. LG organizzative e raccomandazioni per la Rete Oncologica»(48). Qui il coinvolgimento, espresso nei termini di “coinvolgimento istituzionale”, “prevede la partecipazione ai livelli rappresentativi e direzionali” per le associazioni operanti in campo oncologico.
In aggiunta, è stato appena emanato (ottobre 2022) l’ “Atto di indirizzo riguardante le modalità di partecipazione ai processi decisionali del Ministero della Salute da parte delle associazioni o organizzazioni dei cittadini e dei pazienti impegnate su tematiche sanitarie” che stabilisce le regole per la “partecipazione” ai processi decisionali del Ministero della Salute degli Enti (associazioni o organizzazioni dei cittadini e dei pazienti impegnate su tematiche sanitarie) per la promozione della salute, riferita a tutte le attività di cui si occupano le Direzioni Generali del Ministero della Salute… Con il termine di partecipazione si intende nel presente Atto un processo articolato, che si può sviluppare con diverse modalità e in differenti momenti, tramite il quale gli Enti vengono coinvolti, tenendo conto della loro esperienza, competenza e capacità di impatto sui diversi settori delle politiche sanitarie, negli specifici percorsi istituzionali di competenza del Ministero della salute”(49).
Sei sono le modalità di “partecipazione” individuate:
• partecipazione nella consultazione;
• partecipazione nella definizione dell’agenda;
• partecipazione nella co-progettazione dell’intervento;
• partecipazione come supporto all’implementazione dei programmi di politica sanitaria;
• partecipazione nella generazione delle evidenze;
• partecipazione come valutazione e monitoraggio;
• partecipazione come possibilità di riesame.
Il termine centrale “partecipazione” è strettamente correlato a “coinvolgimento”, con la finalità di “incrementare, strutturare e valorizzare la partecipazione civica nell’ambito delle attività di competenza dell’Amministrazione.” In tutti i casi qui accennati, il presupposto implicito – o esplicito come nell’Atto di indirizzo per la partecipazione ai processi decisionali del Ministero della Salute – è che gli Enti /Organizzazioni di Pazienti/ Cittadini possiedano competenze ed esperienze. Questo, in ultima istanza, porta a focalizzare nuovamente l’attenzione sulla formazione/educazione per lo sviluppo di profili di competenze idonei a co-programmare, co-progettare e co-valutare, oltre che a rappresentare bisogni e criticità propri della comunità di riferimento. Il requisito di competenza diviene cruciale, per quanto condizione necessaria ma non sufficiente se non connessa ad altre dimensioni, in primis a quella di “esperienza” e “impatto”.
In conclusione:
• “engagement” e “involvement” sono concetti applicabili sia a una dimensione individuale sia collettiva (organizzazioni di pazienti), con riferimento sia al proprio percorso di cura sia a processi di interesse collettivo;
• se “engagement” tende a enfatizzare la dimensione relazionale-sistemica, “involvement” sembra sottolineare maggiormente l’aspetto di “condivisione/cooperazione/partecipazione attiva” sia strategica sia operativa di percorsi/processi/attività;
• la non univocità della terminologia sottolinea l’esistenza di un dibattito aperto in un contesto di interazioni multi-stakeholder ancora in evoluzione;
• considerata l’eterogeneità dei processi/attività, ciò che rimane essenziale è sempre una chiara specificazione degli ambiti e dei livelli d’intervento, e, ancor prima, delle FINALITÀ/OBIETTIVI da raggiungere e quindi di CHI coinvolgere per ottenere i risultati previsti. Esser coinvolti nel disegno di un protocollo di ricerca clinica è diverso dall’esser coinvolti nel processo di de nizione di percorsi diagnostico-terapeutico-assistenziali o in attività di valutazione in seno a Comitati Etici o nell’area della valutazione e implementazione delle tecnologie digitali per la salute e più in generale dell’HTA o, ancora, in processi decisionali del Ministero della Salute. Le conoscenze/competenze/esperienze necessarie non possono che esser diverse tra loro e acquisibili tramite percorsi formativi/educativi/ esperienziali diversificati e differenziati.
Bibliografia
1. Tuckett D, Boulton M, Olsen C and Williams A. 1985: Meetings between experts: an approach to sharing ideas in medical consultations. London: Tavistock.
2. The ExpertPatient-a Welcome Way Forward https://www.cmf. org.uk/resources/publications/content/?context=article&id=1061
3. The Expert Patient: a new approach to chronic disease management in the 21st century. Department of Health, 2001. PDF available onlyne at http://www.dh.gov.uk.
4. White Paper, Saving Lives: Our Healthier Nation https://www. gov.uk/government/publications/saving-lives-our-healthier-nation
5. Newman S, Steed L, Mulligan K. Self-management interventions for chronic illness. Lancet 2004; 364: 1523-37.
6. Barlow J, Wright C, Sheasby J, et al. Self-management approaches for people with chronic conditions: a review. Patient Educ Couns 2002; 48: 177-87.
7. Boulet L-P. The Expert Patient and Chronic Respiratory Diseases.Can Respir J 2016; 2016: 9454506 http://dx.doi.org/10.1155/2016/9454506
8. Cordier J-F. The expert patient: towards a novel de nition. Our Respir J 2014; 44: 853–7. DOI: 10.1183/09031936.00027414.
9. Regulation (EC) No 726/2004 of the European Parliament and of the Council of 31 March 2004 laying down Community procedures for the authorisation and supervision of medicinal products for human and vete- rinary use and establishing a European Medicines Agency – https://eurlex.europa.eu/legal-content/EN/TXT/?uri=celex%3A32004R0726
10. European Medicines Agency stakeholder relations management framework (EMA/48651/2016) https://www.ema.europa.eu/en/committees/working-parties-other-groups/chmp/patients-consumers-working-party
11. Engagement Framework: EMA and patients, consumers and their or- ganizations” (EMA/649909/2021), https://www.ema.europa.eu/en/partners-networks/patients-consumers#activities-of-patients-and-consumers-section
12. How the European Medicines Agency interacts with patients and con- sumers. presentation-how-european-medicines-agency-interacts-patients-consumers_en
13. Getting involved https://www.ema.europa.eu/en/partners-networks/patients-consumers/getting-involved
14. Involvement in EMA activities: registration for interested individuals; https://fmapps.ema.europa.eu/stakeholders/signup.php
15. Stakeholders and Communication Division EMA individual experts’ stakeholder database: patients and consumers- Frequently asked questions, https://www.ema.europa.eu/en/documents/other/ema-individual-experts-stakeholder-database-patients-consumers-frequently-asked-questions_en.pdf
16. Patients and Healthcare Professionals Training strategy for pa- tients and consumers involved in EMA activities (11 November 2014 EMA/664931/2014 Rev. 1)
17. European Patients’ Academy on Therapeutic Innovation (EUPATI); https://eupati.eu/?lang=it
18. https://eupati.eu/about-us/10-years-of-eupati/
19. EUPATI Training Portfolio https://eupati.eu/training/
20. EUPATI Patient Expert Training Programme Guidelines 2022 –2023; https://learning.eupati.eu/mod/page/view.php?id=438
21. Principles of successful Patient involvement in CANCER research (Berlin Declaration- EU against cancer- Initiative of the Trio Presidency of the EU council Germany, Portugal, Slovenia; https://www.bmbf.de/SharedDocs/ Downloads/en/210907-unite-against-cancer.pdf?_blob=publicationFile&v=2
22. Baldwin MA (2003) Patient advocacy: a concept analysis. Nurs Stand 2003; 17: 33-9.
23. Meleis AI. Theoretical nursing development and progress (3rd ed.). 1997 Lippincot- Raven, Philadelphia.
24. Archer Copp L. The nurse as advocate for vulnerable persons. J Adv Nurs 1986; 11: 255-63.
25. Bawden R. & Lindsay E. Patient Empowerment: a general practi- ce perspective. Br J Community Nurs 2007; 12: S28-30.
26. Gonzalez AR. Patien Advocacy History. Evolution and Impact on Health.JOJ PubHealth 2018;3(3):555615.DOI:10.19080/JOJPH.2018.03.55561
27. https://www.cancer.gov/publications/dictionaries/cancer-terms/def/patient- advocate
28. https://www.cancer.gov/publications/dictionaries/cancer-terms/ def/patient-navigator
29. Farrer L, Marinetti C, Kuipers Cavaco Y, Costongs C. Advocacy for Health Equity: A Synthesis Review. Milbank Q 2015; 93: 392-437.
30. European Patient Forum- The added value of patient organiza- tions Dorota Sienkiewicz, Corine van Lingen Editors: Nicola Bedlington, Camille Bullot, Kaisa Immonen Published: November 2017
31. Scher DL. How patient-centric care differs from patient-centered care. The Digital Health Corner https://davidleescher.wordpress.com/2012/03/03/ how-patient-centric-care-differs-from-patient centered-care-2/
32. M. Anderson, M. Manganiello. Back to basics: HIV/AIDS Advoca- cy as a Model for Catalyzing Change. (FasterCures, Washington, DC, 2011).
33. Wilson R. The challenge of sarcomas: the patient advocacy group perspective. Clin Sarcoma Res 2019; 9: 11.
34. Wong-Rieger D. Moving from patient Advocacy to Partnership: A Long and Bumpy Road. Patient 2017; 10: 271- 6. doi: 10.1007/s40271-017-0216-1.
35. “Patient-Focused Drug Development Glossary Standardized no- menclature and terminologies related to patient-focused medical product development (2018) https://www.fda.gov/drugs/development-approval-process-drugs/patient-focused-drug-development-glossary
36. https://www.fda.gov/regulatory-information/selected-amendments-fdc-act/21st-century-cures-act
37. ICH reflection paper – proposed ICH guideline work to advance Patient Focused Drug Development (PFDD), – Committee for Medicinal Products for Human Use- EMA/CHMP/ICH/338534/2021
38. Codice Deontologico Farmindustria, 5 aprile 2022; https://www. farmindustria.it/app/uploads/2018/06/2022-APRILE-5.pdf
39. Staley K, Elliott J, Stewart D, Wilson R. Who should I involve in my research and why? Patients, carers or the public? Res Involv Engagem2021; 7: 41. doi: 10.1186/s40900-021-00282-1.
40. Jackson T, Pinnock H, Liew SM, Horneet E, et al. Patient and pu- blic involvement in research: from tokenistic box ticking to valued team members. BMC Med 2020; 18: 79. doi: 10.1186/s12916-020-01544-7.
41. Graffigna G, Barello S, Riva G, Castelnuovo G, et al. Promozione del patient engagement in ambito clinico-assistenziale per le malattie croniche: raccomandazioni dalla prima conferenza di consenso italiana. Re- centi Prog Med 2017; 108: 455-75.
42. Briefing notes for researchers – public involvement in NHS, health and social care research https://www.nihr.ac.uk/documents/brie ng-notes-for-researchers-public-involvement-in-nhs-health-and-social-care-research/27371-
43. Regulation (EU) No 536/2014 of the European Parliament and of the Council of 16 April 2014 on clinical trials on medicinal products for human use, OJ L 158, 27.5.2014, p. 1-76, Annex I
44. Dockser Marcus A. To make progress in rare cancers, patients must lead the way. J Clin Oncol 2009; 27: 2575-7.
45. Gonzato O, Gronchi A. The evolving role of patient advocates in rare cancers: opportunities and challenges. Expert Rev Pharmacoecon Out- comes Res 2019; 19: 1-3.
46. STAMP Working Group- Proposal for a framework to support not-for-pro t organisations in drug repurposing https://health.ec.europa. eu/system/ les/2019-04/stamp_11_47_2_en_0.pdf
47. Decreto Legislativo 3 luglio 2017, n. 117. Codice del Terzo settore- https://www.lavoro.gov.it/documenti-e-norme/normative/Documents/2017/ Decreto-legislativo-03072017-n-117-Codice-del-Terzo-settore.pdf
48. Atto n. 59/CSR –17/04/19 – Revisione delle Linee Guida organizzative e delle raccomandazioni per la Rete Oncologica che integra l’attività ospedaliera per acuti e post acuti con l’attività territoriale.
49. Atto di indirizzo riguardante le modalità di partecipazione ai pro- cessi decisionali del ministero della salute da parte delle associazioni o or- ganizzazioni dei cittadini e dei pazienti impegnate su tematiche sanitarie- https://www.salute.gov.it/imgs/C_17_pubblicazioni_3265_allegato.pdf



